|
尊敬的患者朋友:
一项由本公司之附属公司泰州复旦张江药业有限公司(以下简称“泰州复旦张江”)申办的口服盐酸氨酮戊酸口服溶液用粉末(以下简称“该药物”)对恶性脑胶质瘤进行光动力诊断的III期临床试验研究(以下简称“本研究”)正在有关医院神经外科开展,本研究的实施已经得到有关医院伦理委员会的批准。
现招募符合以下条件的恶性高级别(WHO 3~4 级)脑胶质瘤患者:
药物介绍
泰州复旦张江就该药物于2023年12月获得药物临床试验申请受理通知书,并于2024年3月获得临床试验批件。该研究旨在评价恶性高级别(WHO分级3-4级)脑胶质瘤患者口服盐酸氨酮戊酸口服溶液用粉末(5-ALA)用于荧光引导下肿瘤切除术的有效性和安全性。
研究介绍
本研究已获得国家药品监督管理局(NMPA)和参与本研究的医院伦理委员会的批准。目前全国多家医院正在为本研究招募患者,预计将招募总计约80例的高级别脑胶质瘤患者。
入选标准
- 疑诊或确诊为恶性高级别脑胶质瘤(WHO3~4级);经研究者评估受试者适合进行脑胶质瘤肿瘤切除术,且术前评估能达到肿瘤完全切除,即病灶可以被完全切除而不会因此影响重要生理功能
- Karnofsky功能状态(Karnofsky performance status KPS)评分≥70;预计生存时间≥3个月
- 既往抗肿瘤治疗(包括手术)的所有毒性反应缓解至基线严重程度或恢复至≤NCI
CTCAE v5.0定义的1级脱发、周围神经病变可为≤2级
参研医院
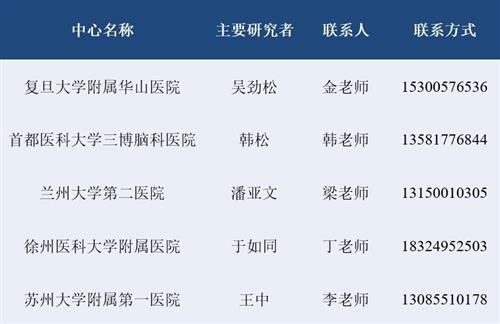
注:如果您希望了解更详细的信息或有兴趣参与本研究,可就近向上述研究中心进行咨询。在您正式参加研究前,院方会向您详细介绍研究内容,并征得您的书面同意。
声明
本文仅作招募信息转发,患者报名资料将由上述研究中心直接进行审核与对接,为严格遵守隐私保护法规,确保患者信息安全,本文不开设留言及私信功能。参与研究存在风险与不确定性,敬请患者朋友谨慎决策。感谢您的关注与支持。
|

 沪公网安备31011502002670号 (沪)-非经营性-2024-0273
沪公网安备31011502002670号 (沪)-非经营性-2024-0273  沪ICP备10027510号-1
沪ICP备10027510号-1